2023年6月20日,浙江大学动物科学学院王迪铭副教授、蔡杰研究员联合材料科学与工程学院邓人仁研究员团队在Nature Communications上发表题为Antioxidant hepatic lipid metabolism can be promoted by orally administered inorganic nanoparticles(https:// doi: 10.1038/s41467-023-39423-3)的研究论文,该最新研究成果揭示了利用纳米微量元素促进羧酸酯酶介导抗氧化性肝脂肪代谢,并阐明了其关键分子机制。
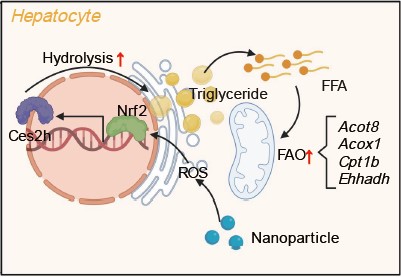
肝脏是哺乳动物的代谢中心,肝脏代谢稳态维持对机体整体营养、生理和健康具有重要意义。研究人员首先发现,纳米微量元素主要被肝Kupffer细胞捕获,并经过Kupffer细胞-肝实质细胞传递留存于肝实质细胞中的内质网-线粒体系统中,随后通过产生一定水平的氧自由基(ROS)来激活细胞内核红细胞2相关因子2(Nrf2);进一步结合转录组学分析、基因编辑技术、分子对接分析和生化实验,发现肝实质细胞内Nrf2的激活通过信号级联诱导了其下游羧酸酯酶(Ces2h)基因的表达,并介导肝脏的酯水解和脂代谢作用。为进一步探究Nrf2如何参与肝实质细胞中Ces2h介导的酯水解和脂代谢作用,团队在动物和细胞模型中实施了羧酸酯酶基因敲除,发现羧酸酯酶可通过清除ROS来促进肝脏脂解作用。为明确羧酸酯酶基因介导肝脏中ROS清除和脂代谢作用的分子机制,我们对CES2/Ces2h进行了同源建模和分子对接分析,结果表明,当引入特定ROS——羟自由基(·OH)时,羧酸酯酶与其底物——酯的相互作用和催化能力都有所提高。且通过点突变构建异常羧酸酯酶——CES2p.G193A和 Ces2hp.G148A后,发现这些突变体通过阻止·OH的进入而降低酯催化活性。生化实验进一步证明羧酸酯酶在有·OH情况下,通过消耗·OH加速酯催化过程。因此,羧酸酯酶介导了抗氧化型脂肪代谢。进一步研究发现,纳米微量元素不仅可通过激活Nrf2-羧酸酯酶级联效应增加肝脏中的酯水解解作用,还可通过调节PPAR‐α以及其下游基因(Cpt1b、Ehhadh、Acox1和Acot8),促进肝脏中的脂肪代谢。
本研究通过搭建生命科学和物质科学的“立交桥”,揭示了抗氧化功能参与肝脏脂肪代谢调节的作用机制,丰富了动物代谢调控理论。相关成果可为研发兼具应激缓解和代谢干预的营养调控技术提供新思路,助力奶牛等畜禽的绿色健康养殖模式构建。
浙江大学动物科学学院为论文第一作者单位和通讯作者单位。王迪铭副教授为通讯作者,蔡杰研究员为第一作者。材料科学与工程学院邓人仁研究员和动物科学学院蔡杰研究员为论文共同通讯作者,材料科学与工程学院博士生彭洁、动物科学学院博士生冯娟为论文的共同第一作者,浙江大学动物科学学院刘建新教授、环境与资源学院王娟研究员、医学院附属第一医院赵鹏教授等对本研究给予了大力帮助。研究获得了国家自然科学基金委 (31930107, 32172741, 32102552, T2122003, 52173290)等项目的支持。
(文 蔡杰)
科研科
2023年7月5日


