肠道菌群能够通过短链脂肪酸等代谢产物调控宿主的抗病毒天然免疫应答。人参等中草药的活性单体成分具有调节肠道菌群及抗病毒感染等多种生物学功能,然而相关机制并未得到完全解析。近年来,由肠道病毒感染导致的公共卫生问题日益凸显,不仅造成昂贵的医疗支出,还导致一定程度的重症感染和死亡。由于临床缺乏高效的商业化疫苗及抗病毒药物,因此,能否通过中药单体以调节肠道菌群的方式诱导宿主抗病毒天然免疫,是肠道病毒防控及治疗中亟待回答的重要科学问题。
近日,“百人计划”研究员朱书团队在The ISME Journal杂志上发表题为“人参皂苷Rg3通过产短链脂肪酸共生菌调控宿主cGAS-STING-IFN-I轴拮抗肠道病毒感染”的研究工作。该工作以鼠源诺如病毒(MNV-1)及脑心肌炎病毒(EMCV)为模式肠道病毒建立小鼠感染模型,发现在体外无抗病毒作用的人参皂苷单体Rg3,在饲喂小鼠后通过富集肠道中产短链脂肪酸的布劳特菌拮抗肠道病毒的局部及全身性感染。进一步通过转录组分析及体内外试验,证实布劳特菌代谢产物乙、丙酸能够通过巨噬细胞表面G蛋白偶联受体43(GPR43),促进细胞内Ca2+水平升高,并与病毒感染导致的线粒体DNA外溢协同激活cGAS-STING通路,促进下游IRF3磷酸化和 IFNβ的表达,增强抗病毒天然免疫应答。该工作原创性地揭示了布劳特菌代谢产物乙、丙酸通过GPR43-cGAS-STING-IFN-I轴诱导宿主抗肠道病毒天然免疫的分子机制。提示人参皂苷Rg3及布劳特菌可成为预防或治疗肠道病毒感染的候选微生态制剂,为临床治疗肠道病毒感染提供新的治疗方案和思路。

研究者首先使用人参皂苷Rg3预处理小鼠,以局部感染的鼠诺如病毒(MNV-1)和全身性感染的脑心肌炎病毒(EMCV)作为肠道病毒感染模型,采集感染时小鼠的粪便样品,经16S rRNA测序分析发现,人参皂苷Rg3处理组,其布劳特菌属丰度较高,其病毒拷贝数显著降低。使用Vancomycin清除肠道菌群后的野生型小鼠,或使用无菌小鼠,证实布劳特菌单菌定植能够拮抗MNV-1的局部感染,改善了因EMCV感染导致的小鼠病理损伤,并显著提高了存活率。
短链脂肪酸是指六个碳原子以下的有机脂肪酸,包括乙酸,丙酸和丁酸等。主要来源于结肠中厌氧细菌对肠道内纤维和不可消化糖的发酵。作为肠道微生物的重要代谢产物,具有为动物体提供能量、调节能量代谢、参与信号转导、改善心血管疾病、缓解糖尿病病症、维持肠道代谢完整性、调节肠道菌群和免疫功能调控等多种生物学功能。然而,前人研究从未发现产短链脂肪酸共生菌布劳特菌的代谢产物乙、丙酸对于激活宿主抗肠道病毒天然免疫的重要作用。
研究者对人参皂苷Rg3处理或布劳特菌单菌定植的小鼠粪便进行靶向代谢组分析发现,处理组小鼠粪便中乙、丙酸水平显著升高。通过动物试验和细胞试验,转录组分析等,证实乙、丙酸通过巨噬细胞表面受体GPR43,以细胞内Ca2+和线粒体抗病毒信号蛋白(MAVS)依赖的方式,促进线粒体通透性转换孔道的开放,线粒体DNA(mtDNA)的释放,从而激活cGAS-STING-IFN-I轴,诱导宿主抗肠道病毒天然免疫。
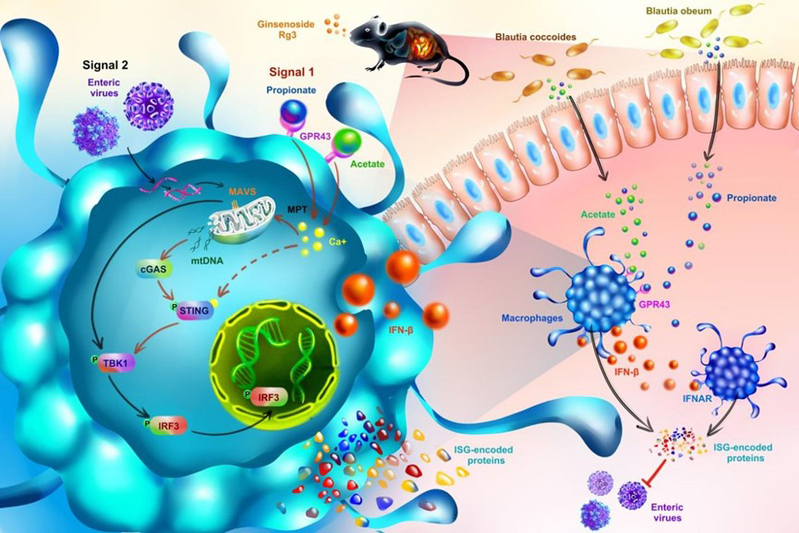
Figure: Schematic illustration of how the Blautia spp.-associated metabolites acetate and propionate protect against enteric virus infection through the GPR43-cGAS-STING-IFN-I axis.
如模式图所示:人参皂苷Rg3给药正常小鼠后,肠道中布劳特菌大量富集。其代谢产物乙、丙酸作用于巨噬细胞表面受体GPR43,提高细胞内Ca2+水平。当病毒入侵宿主时,线粒体上的MAVS被激活。在乙、丙酸以及病毒的双重信号作用下,线粒体通透性转换孔道的开放程度增加,mtDNA外溢增强,从而激活下游cGAS-STING-IFN-I信号通路,促进干扰素刺激基因(ISGs)的表达,进而产生抗病毒蛋白,拮抗肠道病毒感染。
博士生王干为论文第一作者,朱书研究员为论文通讯作者。该工作受到国家自然科学基金会(32172864和U21A20261)的资助。
朱书团队供稿
2023年11月21日

